吉林長春長生生物科技公司(長生生物)問題疫苗事件持續發酵。內地媒體深挖發現,過去十年,中國疫苗從研發、生產、銷售、採購等所有環節幾乎都被貪腐侵蝕,而涉事的長生生物去年支出4.42億元(人民幣,下同)巨額「推廣服務費」,疑似用於子公司長春長生員工、經銷商向地方醫院、疾病防疫部門行賄,以推銷產品。

安徽黃山在屯溪區疾控中心昨日就地封存的長春長生凍乾人用狂犬疫苗。 (CFP圖片)
觸目驚心的疫苗亂象拷問中國藥品監管制度,媒體指出,不僅中國對部分疫苗的檢驗標準低於國際水平,而且對製藥企業違法懲罰力度太輕,讓廠商肆無忌憚的造假,戕害消費者。
長生生物年報顯示,2017年全年,長生生物營業總成本為9.67億元,其中銷售費用5.83億元,銷售費用在營業成本中的佔比高達60.29%。但銷售人員僅25人,人均銷售費用2,331.85萬元。那長生生物銷售費用都用於何處呢?年報顯示,其中4.42億元為「推廣服務費」,並解釋是子公司長春長生向推廣服務公司支付的費用。
但據澎湃新聞網通過梳理裁判文書網判決資訊發現,過去十年,長春長生員工、經銷商在疫苗銷售過程中,涉及多宗行賄,其通過行賄地方醫院、疾病防疫部門,給予回扣方式推銷其產品。例如2002年至2003年,長春長生原安徽區經理班某與蒙城縣防疫站站長和採購約定,每銷售一份甲肝疫苗,就給0.5元回扣。蒙城縣防疫站兩年接種12.7萬份甲肝疫苗,班某給予站長和採購60,000元「好處費」。有業內人士感嘆:「你不給(回扣)又怎麼會用你的東西(疫苗)呢?」報道指出,疫苗腐敗的另一模式是無資質的疫苗銷售機構,或生產銷售不合格疫苗的企業或個人,直接賄賂相關官員,致使不合格疫苗流入市場。2016年著名的「山東假疫苗事件」,在全國範圍內便有多名官員被追究刑事責任。另外,還有疫苗研發企業為在生產研發階段獲得支持,賄賂藥品主管部門官員。
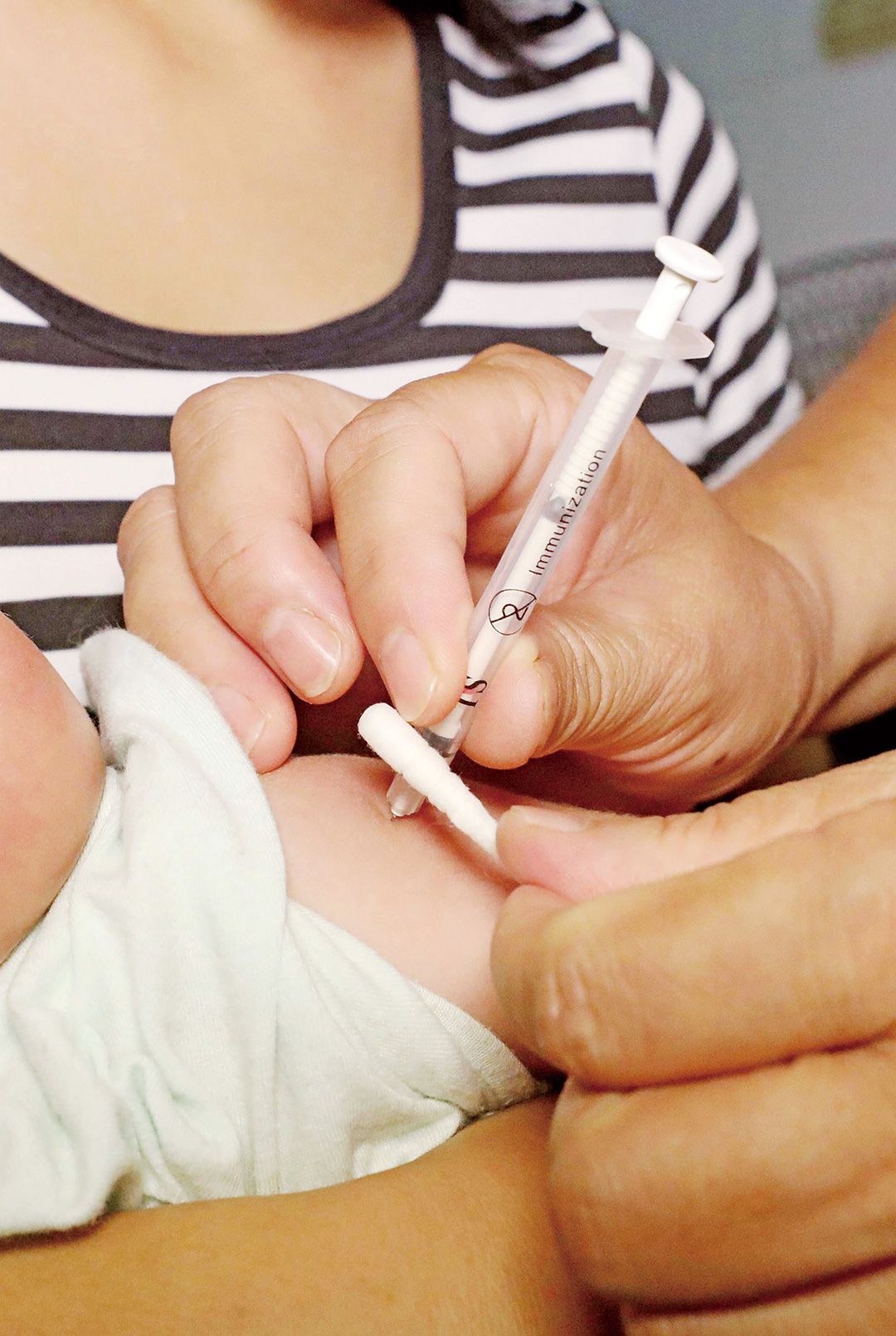
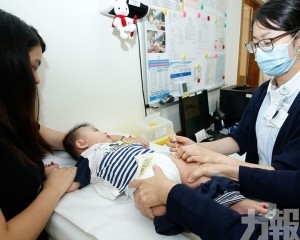
廣西柳州,融安縣長安鎮衛生院,一名醫護人員在為兒童接種疫苗。 (CFP圖片)
疫苗檢驗標準低於國際水平
疫苗腐敗問題觸目驚心,外界質疑監管部門難辭其咎。據了解,中國從2006年起就已經實現對所有疫苗的批簽發管理,每批製品出廠上市或者進口時都要進行強制性檢驗、審核。但批簽發只檢測疫苗安全性,對於有效性的檢測,中國按照國際慣例只進行抽檢。自2008年以來,國家藥品監管部門開展疫苗評價性抽驗,即從生產、流通和使用三個環節抽取疫苗產品進行品質核對總和結果分析。但據《第一財經》報道,行業內資深人士表示,中國對部分疫苗的檢驗標準低於國際水平,雖然不少疫苗都採取三次抽驗的方式進行評價性抽驗,但三次抽驗中有一次通過即可,但在國際上很多國家採取的是三次抽檢必須全部通過。

廣西柳州融安縣疾病預防控制中心疫苗倉庫,市場監督管理局執法人員對存儲疫苗進行檢查。(CFP圖片)
處罰力度被質疑太輕
不僅是監管與國際標準有出入,藥企違法成本太低亦成為公眾質疑的焦點。就此次長生生物疫苗事件的處罰而言,國家藥品監督管理局對違法違規生產的凍乾人用瘋狗症疫苗,僅作出收回該企業《藥品GMP證書》,責令停止瘋狗症疫苗生產的處罰決定。而在去年11月被發現的「百白破」問題疫苗,吉林省食品藥品監督管理局直到九個多月後的今天,才下發行政處罰決定書,在共計25萬支流入市場的前提下,僅做出沒收186支庫存疫苗,罰款344萬元的處罰決定。這樣的處罰力度被民眾認為等於縱容企業繼續作惡,企業很快就會有第二次、第三次造假。
近年重大疫苗安全事故
2016年山東疫苗事件
2016年3月,山東警方破獲案值5.7億元疫苗非法流通案,涉案12種疫苗約200萬支,未經合格的冷藏儲運,銷往全國24個省市。事後,多名官員被追究刑事責任。
2013年乙肝疫苗致死事件
2013年11月至12月,南方地區發生多宗嬰兒注射乙肝疫苗後致傷致死的事件。事後,多家乙肝疫苗生產企業陷入風波。但最後當地醫療主管部門認定死亡為「偶合症」(受種者正處於某種疾病的潛伏期,接種後巧合發病)。
2010年山西疫苗事件
2007年,山西發生多宗兒童注射疫苗後致傷致死的事件。事件2010年被《中國經濟時報》首席記者王克勤揭露。山西官方認為報道不實,但事件仍引起全國性的對官方疫苗安全的質疑。
2009年廣西來賓假狂犬疫苗事件
2009年12月,來賓市一名五歲男童被狗咬傷後到鄉衛生院打瘋狗症疫苗,但21天后病發死亡。經化驗,所用瘋狗症疫苗為假藥。來賓市調查發現當地非法管道進購藥品犯罪鏈,查獲「問題」人用瘋狗症疫苗1,000多人份,貨值33萬多元,拘捕八名疑犯。
逾20省份回應疫苗流向
上海: 已全面停用長春長生瘋狗症疫苗。上海疾控中心稱,如已接種過長春長生瘋狗症疫苗部分劑次,可選擇其他品牌瘋狗症疫苗。
河南: 河南全省上報封存的長春長生瘋狗症疫苗數量是14萬1,380.8人份(每人份是五支),佔長春長生瘋狗症疫苗河南市場總量的90%以上。
山東: 山東疾控稱,長春長生公司生產的流入山東的25萬2,600支不合格百白破疫苗(批號201605014-01),流向已全部查明,涉及兒童未發現疑似預防接種異常反應增高。
重慶:暫停使用並就地封存長春長生瘋狗症疫苗。
廣西: 今年全區採購系統中瘋狗症疫苗配送量為150萬支,長生生物配送量為48 萬支,已有58 個縣(市、區)召回93,384支。
海南:已全面停用長春長生瘋狗症疫苗。
西藏: 從未在長春長生購買「人用瘋狗症疫苗」和「吸附無細胞百白破聯合疫苗」,與該公司無任何業務關聯。
浙江:長春長生公司通知召回原批准上市的瘋狗症疫苗,已全部封存。
廣東:無長春長生公司涉事批次的瘋狗症疫苗。
江蘇: 揚州市少部分使用長春長生公司疫苗的地區,已經採取措施進行處理。
北京:長生生物這兩個出問題的疫苗,北京市均未採購。
四川:問題凍乾人用瘋狗症疫苗已全部實施召回,並未進入社會。
河北: 長春長生生產的瘋狗症疫苗在河北省的採購目錄之內,目前全省各地疾控機構已經全面停用並封存該企業生產的狂犬疫苗。