這項臨床試驗旨在研究復必泰疫苗在中國健康人群中的安全性和免疫原性。
內地媒體《財新網》報道,復星醫藥與德國疫苗公司BioNTech合作的復必泰疫苗在內地完成二期臨床研究,朝著進入內地市場再邁進一步。
據美國臨床試驗數據庫顯示,5月10日,復必泰在內地的臨床試驗更新了研究進展,II期臨床試驗的狀態從「進行中」變更為「已完成」,這項臨床研究在2022年1月9日完成。
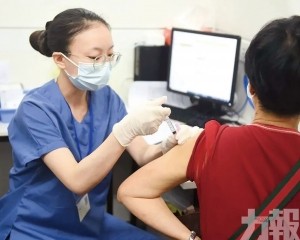
這項臨床試驗旨在研究復必泰疫苗在中國健康人群中的安全性和免疫原性,參與試驗的有950人,年齡在18至85歲之間,由復星醫藥於2020年12月負責開展,試驗地在江蘇省疾病預防控制中心。
據德國證券網站「BÖRSE ONLINE」報道,BioNTech一名發言人對此稱,「我們已向(中國)相關主管部門提交了一份全面的數據包,主管部門正在審閱文件,並根據這些數據評估疫苗,結果將由當局宣布」。財新網報道又指,一般而言,新冠疫苗要在國內上市,都要經過臨床前試驗、I至III期臨床試驗、註冊審批等流程。
由於復必泰已在國外進行過III期臨床,積累了大量數據,流程上可以簡化。復星醫藥曾表示,復星醫藥計劃以橋接方式結合復必泰在海外進行的III期臨床試驗結果,一起向國家藥品監督管理局報批上市。這意味著,這款疫苗在海外積累的數據可以和II期臨床試驗結果一併提交,無需重複III期臨床。(編輯:麥敏楨)