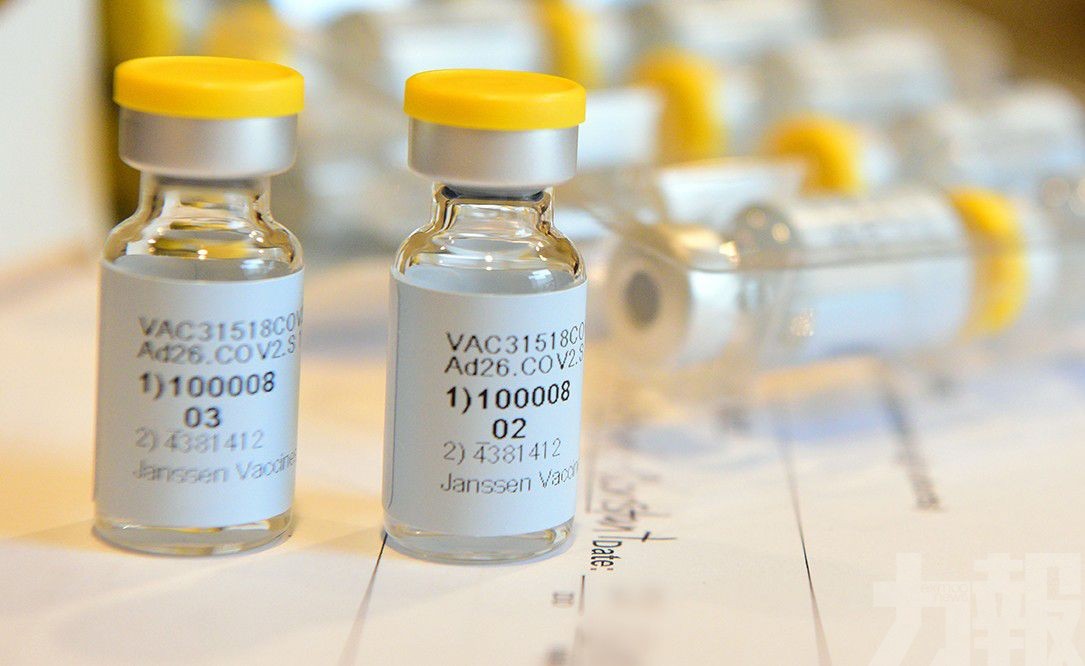
美國強生公司已向美國食品及藥物管理局申請緊急授權自家研發的新冠疫苗上市。(Johnson & Johnson官網圖片)
美國強生公司(Johnson & Johnson)周四(4日)宣布,已向美國食品及藥物管理局(FDA)申請緊急授權自家研發的新冠疫苗上市。如果獲批准,將會是第三款獲准在美國緊急授權使用的疫苗。
此前獲批的美國輝瑞(Pifizer)和莫德納(Moderna)疫苗均需接種兩劑,而強生的只需打一劑,並可在雪櫃溫度下儲存至少三個月,更方便運送和分發,若在零下20攝氏度下更可儲存兩年之久。
強生表示,已準備好在獲批後即刻運送疫苗作緊急使用,預計可在今年七月前向全美供應一億劑,亦計劃每年生產10億劑,會在未來數周向歐洲藥物管理局申請使用許可。美國過敏與感染疾病中心主管福奇表示,若強生疫苗獲FDA批准使用,將在三月上市。
強生於1月29日發表臨床試驗報告,這款疫苗在大型全球試驗的有效性為66%,可預防85%的嚴重感染,對於預防住院和死亡的有效率更是達到100%(編輯:陳妙芝)